Capítulo 1: Carga Elétrica
Carlos Alberto dos Santos, Eliabe Maxsuel de Aquino, Geovani Ferreira Barbosa
Universidade Federal Rural do Semi-Árido
Mestrado Nacional Profissional em Ensino de Física
Você viu nos Organizadores Prévios, que os dois conceitos mais importantes da eletricidade são a carga elétrica e o campo elétrico. A carga elétrica gera um campo e a partir daí seguem-se todos os fenômenos da eletricidade. Vamos tratar neste capítulo especificamente da carga elétrica. De onde ela surge e como os corpos podem ser eletricamente carregados.
De acordo com os conhecimentos da física contemporânea, a carga elétrica na natureza é transportada por diferentes tipos de partículas elementares, sendo, nesse contexto, o elétron a principal delas. Embora muito importantes para a física das partículas elementares, os léptons e os quarks não precisam ser considerados em uma abordagem elementar da eletricidade. Ou seja, vamos nos concentrar aqui tão somente no elétron e no próton, que não é uma partícula elementar, mas é constituída de quarks que lhe conferem uma carga elétrica igual em valor e oposta em sinal à carga do elétron.
Sabemos hoje que essas partículas, juntamente com os nêutrons são os componentes básicos do átomo. Embora a humanidade tenha mais de 130 mil anos de existência, desde o surgimento do homo sapiens, ou mais de 5 mil anos desde os egípcios, ou mais de 4 mil anos desde os gregos, essa ideia de que o átomo é constituído de prótons, nêutrons e elétrons só foi consolidada entre 1897 e 1932.
Em 1897, Joseph John Thomson descobriu que a carga negativa que se observava em diversos experimentos da física era transportada por uma partícula que George Francis Fitzgerald sugeriu ser denominada elétron, porque em 1891, George Johnstone Stoney tinha usado esse termo para designar a unidade de carga em experimentos nos quais ele passava corrente elétrica através de produtos químicos.

Entre 1908 e 1911, Ernest Rutherford, realizou experimentos que o levaram a propor o modelo atômico que foi desenvolvido por Niels Bohr. Neste modelo, o átomo seria constituído de um núcleo muito pequeno e pesado, em torno do qual orbitariam os elétrons.
Em 1919, Rutherford descobriu que o núcleo continha uma partícula que ele denominou próton, com carga elétrica positiva e muito mais pesada que o elétron, mas que poderia conter outra partícula, neutra, com massa similar à do próton.

Em 1932, seu colaborador James Chadwick descobriu essa partícula, que foi denominada nêutron.
Mas, para chegar a esta fase gloriosa de 35 anos (1897–1932), filósofos e cientistas, desde os gregos, como Tales de Mileto (625–547 a.C.) e Aristóteles (384–322 a.C.), até John Dalton (1766–1844), desenvolveram vários modelos atômicos. Esses modelos fazem parte da história, e não é objetivo nesta disciplina estudá-los. Eles são apresentados nas disciplinas de química. Aqui usaremos apenas o modelo de Bohr, sugerido por Rutherford.

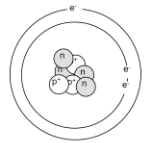
Resumindo tudo isso, podemos dizer que a matéria é constituída de átomos, e que esses são constituídos de um núcleo muito pequeno, contendo prótons e nêutrons, em torno do qual, em grandes distâncias, orbitam os elétrons. Do ponto de vista atômico, podemos dizer que a matéria é um grande vazio. Mas, o que interessa para a nossa disciplina, é que a carga positiva se concentra no núcleo, e a carga negativa fica ziguezagueando em torno dele. Em condições normais, o átomo é eletricamente neutro, porque o número de prótons é igual ao de elétrons.
Podemos imaginar que nesse modelo a força de atração entre prótons e elétrons é a força coulombiana que você vai estudar no próximo capítulo, e vai ver que os elétrons mais afastados do núcleo são fracamente atraídos por ele, de modo que podem facilmente sair do átomo. Esses elétrons livres são os responsáveis pela corrente elétrica nos condutores
Quando um elétron sai do átomo, ele o deixa com um próton a mais do que o número de elétrons, de modo que agora o átomo é positivo. Os átomos que perdem elétrons são denominados íons. Eles estão ionizados.
Se esses elétrons menos ligados ao núcleo podem se liberar do átomo, eles também podem passar de um corpo a outro? Podem.
Essa passagem dá origem ao que denominamos de processos de eletrização e condutividade. Os relâmpagos que vemos nas nuvens resultam de processos de transferência de cargas elétricas entre elas. O funcionamento dos diversos motores e equipamentos eletrônicos decorre da condutividade elétrica, ou seja, do movimento de elétrons no interior dos condutores e dos semicondutores.
